La PQQ ou pyrroloquinoléine quinone, parfois appelée méthoxanine, est un composé de la famille des ortho-quinones, qui a été découverte pour la première fois en 1960 chez les bactéries. La première fonction de la PQQ qui a été découverte est une fonction de cofacteur pour des activités enzymatiques bactériennes (activités déshydrogénases). La structure de la molécule sera décrite et isolée quelques années plus tard, en 1979.
Cette molécule est retrouvée de manière universelle chez certaines bactéries, levures ainsi que chez les plantes et les animaux où elle joue en particulier un rôle de facteur de croissance. La PQQ a été retrouvée dans de nombreux fluides biologiques chez les mammifères, comme le plasma, le liquide synovial, la bile ou encore dans le colostrum et le lait.
La présence de pyrroloquinoléine quinone a également été mise en évidence dans des particules de poussières interstellaires et soulève la question de l’importance de cette molécule dans l’apparition de la vie sur terre.
Synthèse et sources alimentaires de PQQ :
Bien que la pyrroloquinoléine quinone soit détectée dans de nombreux fluides biologiques et tissus des mammifères, y compris chez l’homme, ce composé n’est pas synthétisé par l’organisme et nos besoins sont uniquement couverts par les apports alimentaires (et éventuellement les compléments). La synthèse de ce composé par le microbiote intestinal n’a d’ailleurs pas été clairement établie.
Jusqu’à présent, la PQQ a été retrouvée dans tous les aliments et notamment ceux d’origine végétale. On en retrouve dans les fruits et les légumes comme les kiwis, la papaye, le persil, les poivrons verts, les tomates, le soja. Un des aliments les plus riches en PQQ est le natto, un plat fermenté traditionnel japonais à base de graines de soja.
Les teneurs des produits alimentaires restent cependant très modestes, allant de l’ordre du nanogramme (ng) à quelques microgrammes (μg).
L’apport alimentaire journalier en PQQ chez les humains est évalué entre 100 et 400 µg, mais ce chiffre ne tient pas compte des dérivés de PQQ, comme les produits de condensation avec des acides aminés (tels que l’IPQ ou imidazolopyrroloquinoline).
Le PQQ est également retrouvé sous forme de compléments alimentaires, en tant qu’ingrédient nutraceutique, c’est-à-dire en tant qu’ingrédient actif (présent dans les aliments et/ou dans la nature) qui a un effet positif sur la santé humaine. L’EFSA, l’agence européenne de sécurité des aliments, a émis en 2017 un avis positif pour la commercialisation de complément de sel disodique de PQQ (sous la marque déposée BioPQQ ou MGCPQQ en Europe) avec une recommandation d’utilisation maximale de 20mg/jour. Le brevet BioPQQ ou MGCPQQ est détenu par la société japonaise Mitsubishi. Actuellement il s’agit de la seule forme de PQQ officiellement autorisée à la consommation dans l’Union Européenne et aux USA.
Par ailleurs la PQQ est souvent proposée dans des compléments alimentaires en association avec la CoQ10 (Coenzyme Q10) avec qui elle agit en complémentarité. Des études (notamment chez l’animal) ont même montré une action synergique de l’administration de la PQQ avec la coenzyme Q10.
Rôles biologiques de la PQQ :
D’abord identifiée comme nécessaire au fonctionnement d’enzymes bactériennes, la PQQ semble aussi avoir un rôle dans de nombreux processus physiologiques chez les mammifères comme dans le développement des nouveau-nés.
En effet des études chez les rongeurs (rats et souris) ont mis en évidence qu’un régime carencé en PQQ provoquait une croissance néonatale retardée des animaux, et que cette croissance répondait d’une manière dose-dépendant à la quantité de PQQ additionné dans le régime.
Un certain nombre d’enzymes dans notre corps interagissent avec la PQQ, comme la lysyl oxidase qui est impliquée dans la maturation du collagène et de l’élastine, protéines retrouvées en grande quantité dans le tissu conjonctif. La PQQ est donc impliquée notamment dans l’intégrité et la santé de la peau. La pyrroloquinoléine quinone interagit également avec la lactate déshydrogénase (LDH) qui est responsable de la conversion du lactate en pyruvate, un substrat énergétique qui une fois convertie en acetyl-CoA viendra alimenter le cycle de Krebs. Le cycle de Krebs correspond en une suite de réactions enzymatiques qui vont permettre la production de coenzymes réduits (NADH et FADH2), qui viendront alimenter le fonctionnement de la chaîne respiratoire mitochondriale, et donc la synthèse d’ATP.
La PQQ joue un rôle au niveau du système immunitaire, puisque l’immunité est compromise lorsque des souris sont soumises à un régime carencé. Le bon fonctionnement des lymphocytes B et T est dépendant de la PQQ.
Cette molécule aurait également la propriété de moduler l’activité de nombreuses voies de signalisation impliquées dans des phénomènes de prolifération cellulaire comme la voie Ras-MAPK, ou encore des voies de signalisation liées aux phénomènes d’apoptose (mort cellulaire programmée). La PQQ aurait également la propriété de stimuler la synthèse de facteurs de croissance tels que le NGF (Nerve Growth Factor), ou encore d’activer le récepteur à l’EGF (Epidermal Growth Factor), appelé EGFR, qui joue un rôle dans la prolifération des cellules épithéliales.
La PQQ jouerait également le rôle d’un antioxydant, au même titre que la vitamine C, la vitamine E ou encore le glutathion, avec un pouvoir réducteur très important lui permettant de s’opposer efficacement aux effets néfastes des radicaux libres (ou espèces réactives de l’oxygène). En effet, elle aurait un pouvoir antioxydant 5000 fois plus efficace que la vitamine C, ou encore des dizaines de fois plus que certains polyphénols tels que les catéchines (qu’on retrouve en particulier dans le thé vert). La pyrroloquinoléine quinone est également capable d’activer des facteurs de transcriptions tels que NRF-1 et NRF-2 qui sont impliqués dans la régulation d’enzymes antioxydantes telles que la SOD (superoxyde dismutase), la CAT (catalase) ou encore la GPx (glutathion peroxydase).
La PQQ joue également un rôle au niveau mitochondrial et il a été montré que le nombre et la taille des mitochondries étaient affectés par une déficience en PQQ, avec une réduction de 30-40% du contenu mitochondrial chez des souris avec un régime déficient en PQQ par rapport aux souris complémentées. Ce rôle pourrait notamment passer par le fait que la PQQ entraîne une augmentation de l’expression de PGC1-alpha, un gène majeur dans la régulation de la biogenèse mitochondriale. En stimulant la biogenèse mitochondriale, cette molécule permettrait donc d’optimiser le métabolisme général de l’organisme et la production d’énergie cellulaire (ATP).
Plusieurs publications scientifiques ont d’ailleurs proposé de considérer la PQQ comme une « nouvelle vitamine », au vu de ses nombreux rôles biologiques, et du fait que cette substance n’est à priori pas synthétisée de manière endogène.
Intérêt de la PQQ en santé humaine :
La PQQ est particulièrement connue pour son rôle dans la synthèse de nouvelles mitochondries, ainsi que sur les phénomènes dynamiques de fusion et de fission mitochondriale dont l’équilibre régule le bon fonctionnement de ces organites.
La PQQ a démontré des actions bénéfiques sur différents organes tels que le cerveau, le cœur le foie et l’intestin dans différentes études chez l’homme et/ou des modèles animaux :
- La PQQ a un effet La PQQ exercerait un effet bénéfique sur la mémoire et les capacités d’apprentissage et sur l’augmentation du NGF (Nerve Growth Factor), un facteur de croissance impliqué dans la régénération nerveuse. La pyrroloquinoléine quinone serait aussi protectrice dans la prévention des maladies neurodégénératives comme pour la maladie d’Alzheimer. En effet, il a été démontré que cette molécule avait la capacité de réduire la formation de fibrilles amyloïdes.
- La PQQ a un effet cardioprotecteur. Dans des modèles animaux d’ischémie-reperfusion (mimant une situation faisant suite à un infarctus du myocarde) la PQQ a montré un rôle protecteur contre les dommages cardiaques induit par un stress oxydatif.
- La PQQ a une action bénéfique sur la sphère hépatique. Cette molécule a démontré une capacité à réduire les dommages chez des souris génétiquement modifiées Dmi-1 KO, qui sont susceptible au développement d’un hépatocarcinone (cancer hépatique). La PQQ protège de manière significative le foie en inhibant le stress oxydatif et en participant à la réparation des dommages causés à l’ADN dans ce modèle. La PQQ a également démontré une action positive sur la réduction de la stéatose hépatique et ses dommages, en augmentant le métabolisme lipidique, et en protégeant le foie contre les dommages oxydatifs liés à la forte accumulation de graisses hépatiques.
- La PQQ aurait également une action bénéfique sur la muqueuse intestinale. En effet dans un modèle d’inflammation induite par des Escherichia coli entérotoxinogène (ECET) chez le porc, la PQQ a réduit les dommages causés par la bactérie à la muqueuse de l’intestin grêle. La PQQ a notamment réduit l’inflammation notamment par le biais de l’inactivation du facteur NF-κB pro-inflammatoire. La PQQ a également permis de réguler positivement le microbiote intestinal colique et de maintenir une production adéquate de butyrate, un acide gras à courte chaine anti-inflammatoire.
Dosages et toxicité :
La dose sans effet nocif observable ou NOAEL en anglais (Non Observed Adverse Effect Level) est la dose la plus élevée d’une substance ne produisant aucun effet nocif observable dans des études de toxicité. Elle a été déterminée à 400mg / kg de poids corporel / jour dans une étude chez le rat. La PQQ même à haute dose n’a pas démontré d’effet génotoxique, c’est-à-dire altérant l’ADN. Le PQQ a été administré à des doses de 20 à 60mg durant 4 semaines à des adultes sains sans effets secondaires. Les différentes données disponibles mettent en avant qu’une dose de PQQ allant jusqu’à 60mg ne présenterait aucun risque chez l’homme, et plusieurs études cliniques ont montré des effets bénéfiques d’une supplémentation.
La plupart des études ont montré des bénéfices pour des doses allant de 10 à 20mg, ce qui reste les dosages couramment recommandés par les professionnels de santé et retrouvés dans les compléments alimentaires. Il n’y a pas de contre-indications connues à l’utilisation de PQQ à l’heure actuelle.
CONCLUSION :
La PQQ est une molécule aux multiples effets bénéfiques et particulièrement conseillée pour les personnes âgées, les personnes souffrant de fatigue chronique ou de problèmes mitochondriaux ainsi  que pour les personnes en convalescence. Les personnes souhaitant améliorer leur métabolisme et leurs performances physiques, ou encore celles qui veulent lutter contre le déclin cognitif et le stress oxydatif peuvent bénéficier de l’apport de cette molécule venue tout droit des étoiles.
que pour les personnes en convalescence. Les personnes souhaitant améliorer leur métabolisme et leurs performances physiques, ou encore celles qui veulent lutter contre le déclin cognitif et le stress oxydatif peuvent bénéficier de l’apport de cette molécule venue tout droit des étoiles.
Dr Christian Boyer – Dr en Biologie / Physiologie Humaine & Micro-nutritionniste
Ses formations
La démarche fonctionnelle appliquée à la prise en charge des troubles du microbiote : SIBO, IMO et SIFO
- Formateur : Dr Christian Boyer
- Durée : 2 jours (14h)
- En classe virtuelle : 5 & 13 Novembre 2025
- Lyon : 5 & 6 Juillet 2025
- Bruxelles (Belgique) : 20 & 21 Septembre 2025
Cas pratiques et stratégies avancées pour les troubles digestifs fonctionnels
- Formateur : Christian Boyer
- Durée : 1 journée (7h)
- En classe virtuelle : Mardi 3 Février 2026
- Voir le programme complet
Références :
Bishop A, Gallop P, Karnovsky M. Pyrroloquinoline quinone: a novel vitamin? Nutr Rev. 1998 Oct;56(10):287-93. doi: 10.1111/j.1753-4887.1998.tb01661.x.
Chowanadisai W, Bauerly KA, Tchaparian E, Wong A, Cortopassi GA, Rucker RB. Pyrroloquinoline quinone stimulates mitochondrial biogenesis through cAMP response element-binding protein phosphorylation and increased PGC-1alpha expression. J Biol Chem. 2010 Jan 1;285(1):142-52. doi: 10.1074/jbc.M109.030130.
EFSA Panel on Dietetic Products, Nutrition and Allergies (NDA), Turck D, Bresson J-L, Burlingame B, Dean T, Fairweather-Tait S, et al. Safety of pyrroloquinoline quinone disodium salt as a novel food pursuant to Regulation (EC) No 258/97. EFSA Journal. 2017;15:e05058.
Huang Y, Chen N, Miao D. Biological effects of pyrroloquinoline quinone on liver damage in Bmi-1 knockout mice. Exp Ther Med. 2015 Aug;10(2):451-458. doi: 10.3892/etm.2015.2532. Epub 2015 May 29. PMID: 26622336; PMCID: PMC4509087.
Huang C, Ming D, Wang W, Wang Z, Hu Y, Ma X, Wang F. Pyrroloquinoline Quinone Alleviates Jejunal Mucosal Barrier Function Damage and Regulates Colonic Microbiota in Piglets Challenged With Enterotoxigenic Escherichia coli. Front Microbiol. 2020 Jul 24;11:1754. doi: 10.3389/fmicb.2020.01754. PMID: 32849383; PMCID: PMC7396494.
Jonscher K, Chowanadisai W, Rucker R. Pyrroloquinoline-Quinone Is More Than an Antioxidant: A Vitamin-like Accessory Factor Important in Health and Disease Prevention. Biomolecules. 2021 Sep 30;11(10):1441. doi: 10.3390/biom11101441.
Jonscher, K. R. & Rucker, R. B. Chapter 13 – Pyrroloquinoline Quinone: Its Profile, Effects on the Liver and Implications for Health and Disease Prevention. in Dietary Interventions in Liver Disease (eds. Watson, R. R. & Preedy, V. R.) 157–173 (Academic Press, 2019). doi:10.1016/B978-0-12-814466-4.00013-6.
Kim J, Kobayashi M, Fukuda M, Ogasawara D, Kobayashi N, Han S, Nakamura C, Inada M, Miyaura C, Ikebukuro K, Sode K. Pyrroloquinoline quinone inhibits the fibrillation of amyloid proteins. Prion. 2010 Jan-Mar;4(1):26-31. doi: 10.4161/pri.4.1.10889. Epub 2010 Jan 4. PMID: 20083898; PMCID: PMC2850417.
Krueger F, Werther W, Kissel J, Schmid E. Assignment of quinone derivatives as the main compound class composing ‘interstellar’ grains based on both polarity ions detected by the ‘Cometary and Interstellar Dust Analyser’ (CIDA) onboard the spacecraft STARDUST. Rapid Commun Mass Spectrom. 2004;18(1):103-11. doi: 10.1002/rcm.1291.
Michael, M. Pyrroloquinoline quinone (PQQ): the next essential nutrient and supplement superstar. Nutrafoods 125–129 (2018) doi:10.17470/NF-018-1013-3.
Murase K, Hattori A, Kohno M, Hayashi K. Stimulation of nerve growth factor synthesis/secretion in mouse astroglial cells by coenzymes. Biochem Mol Biol Int. 1993 Jul;30(4):615-21. PMID: 8401318.
Naveed, M., Tariq, K., Sadia, H., Ahmad, H., and Mumtaz, A. (2017). The Life History of Pyrroloquinoline Quinone (PQQ): A Versatile Molecule with Novel Impacts on Living Systems. Molecular Biology 1, 00005. 10.15406/ijmboa.2016.01.00005.
Ohwada K, Takeda H, Yamazaki M, Isogai H, Nakano M, Shimomura M, Fukui K, Urano S. Pyrroloquinoline Quinone (PQQ) Prevents Cognitive Deficit Caused by Oxidative Stress in Rats. J Clin Biochem Nutr. 2008 Jan;42(1):29-34. doi: 10.3164/jcbn.2008005.
Qiu K, Zhao Q, Wang J, Qi GH, Wu SG, Zhang HJ. Effects of Pyrroloquinoline Quinone on Lipid Metabolism and Anti-Oxidative Capacity in a High-Fat-Diet Metabolic Dysfunction-Associated Fatty Liver Disease Chick Model. Int J Mol Sci. 2021 Feb 1;22(3):1458. doi: 10.3390/ijms22031458.
Rucker R, Chowanadisai W, Nakano M. Potential physiological importance of pyrroloquinoline quinone. Altern Med Rev. 2009 Sep;14(3):268-77.
Stites T, Mitchell A, Rucker R. Physiological importance of quinoenzymes and the O-quinone family of cofactors. J Nutr. 2000 Apr;130(4):719-27. doi: 10.1093/jn/130.4.719.















 fatigue chronique importante. Les médecins du coin restent alors circonspects, ces patients sont en errance médicale… On y découvre alors 2 mères inquiètes mais combatives qui décident de mener l’enquête à bras le corps, elles contactent des scientifiques et ceux-ci recherchent plusieurs causes possibles. Certains enfants reconnaissent avoir été mordus par une tique peu avant l’apparition des symptômes, d’autres n’en ayant aucun souvenir, il faut dire que cette piqûre peut passer inaperçue car elle est indolore. Les épidémiologistes mettent alors en avant la fréquence de ces piqures dans ce comté comparativement au reste de la population américaine…Ils baptisent ce trouble de maladie de Lyme mais restent impuissants face aux causes qui leur sont alors inconnues..Jusqu’à ce qu’un chercheur, Willy Burgdorfer découvre la bactérie responsable des symptômes de la mystérieuse maladie de Lyme en 1982. On a alors donné le nom à cette bactérie Borrélia Burgdorferi.
fatigue chronique importante. Les médecins du coin restent alors circonspects, ces patients sont en errance médicale… On y découvre alors 2 mères inquiètes mais combatives qui décident de mener l’enquête à bras le corps, elles contactent des scientifiques et ceux-ci recherchent plusieurs causes possibles. Certains enfants reconnaissent avoir été mordus par une tique peu avant l’apparition des symptômes, d’autres n’en ayant aucun souvenir, il faut dire que cette piqûre peut passer inaperçue car elle est indolore. Les épidémiologistes mettent alors en avant la fréquence de ces piqures dans ce comté comparativement au reste de la population américaine…Ils baptisent ce trouble de maladie de Lyme mais restent impuissants face aux causes qui leur sont alors inconnues..Jusqu’à ce qu’un chercheur, Willy Burgdorfer découvre la bactérie responsable des symptômes de la mystérieuse maladie de Lyme en 1982. On a alors donné le nom à cette bactérie Borrélia Burgdorferi.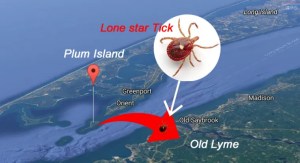


 Ces bactéries ont plus d’un tour dans leur sac afin de n’être ni détectées ni éradiquées.
Ces bactéries ont plus d’un tour dans leur sac afin de n’être ni détectées ni éradiquées. Afin d’avoir une « Happy End », le praticien en santé fonctionnelle sera bien placé afin de « refaire » le film, de comprendre comment cela a commencé et de décortiquer le scénario. Il pourra ainsi davantage démasquer et éradiquer ces imposteurs.
Afin d’avoir une « Happy End », le praticien en santé fonctionnelle sera bien placé afin de « refaire » le film, de comprendre comment cela a commencé et de décortiquer le scénario. Il pourra ainsi davantage démasquer et éradiquer ces imposteurs. 




